概要
本資料では溶液NMRによるタンパク質の構造解析において主鎖解析(T2427)の次のステップである側鎖解析を紹介します。タンパク質(主鎖:-NH-CH(-R)-CO-、側鎖:R)において、主鎖解析では1H-15N HSQCスペクトルのアミドNHピークを帰属したのに対して、1H-13C HSQCスペクトルの各CH結合ピークを帰属することを側鎖解析と呼びます。本解析で得られる情報はNMRによるタンパク質の立体構造解析に必要となります。
タンパク質のNMR解析には貴重な安定同位体(13C, 15N)標識試料が必要となりますが、弊社の700MHz NMR装置に備えた1.7mm Cryoプローブを用いることで通常の1/5未満*の試料量(液量40μL)で測定解析が可能です。
*(株)シゲミ製対称形ミクロサンプルチューブ(5mmφ, 液量200~300μL)との比較
分析方法・分析装置
| 分析方法 | 二次元1H-13C ctHSQC、三次元1H-13C-15N NMR(HBHA(CO)NH, CBCA(CO)NH他) |
| 分析装置 | 700MHz NMR + 1.7 mm Cryoプローブ(1H/13C/15N三重共鳴、インバース型) |
試料
1mMプロテインG B1ドメイン(GB1、13C/15N標識体、6.3kDa) PBS(-)溶液
結果
① タンパク質の1H-13C constant-time HSQCスペクトル
試料の二次元1H-13C constant-time* HSQC(以下ctHSQC)スペクトルを図1に示します。本測定では直接結合した水素と炭素間の相関、すなわちタンパク質中に多数存在するCH結合がそれぞれピークとして検出されます。側鎖解析の目的はこれらのピークを可能な限り帰属(残基番号および位置)することです。
*13C標識試料では、13C-13Cカップリングによるピーク分裂を抑制するため展開時間を一定で測定
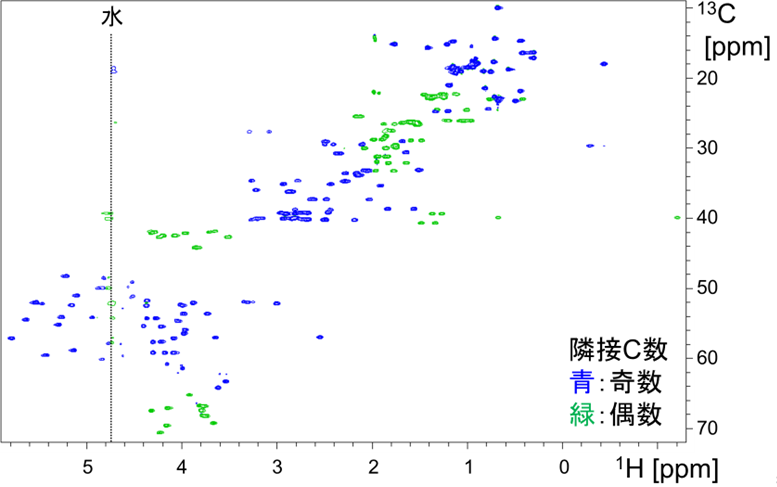
【図1】試料の二次元1H-13C ctHSQCスペクトル(脂肪族領域)
② 三次元NMR測定を用いたタンパク質側鎖解析の概要
側鎖解析に用いる三次元NMR測定では、主鎖解析で得たアミドNHの帰属情報を利用して、アミドNHからカルボニル基を通して一残基前の側鎖の水素または炭素を検出します(図2)。一つのアミドNHから複数のピークが検出されるため、帰属を容易にする目的で、i)α位とβ位のみを検出する測定、およびii)側鎖末端までの全ピークを検出する測定、とそれぞれ三次元測定を行います。
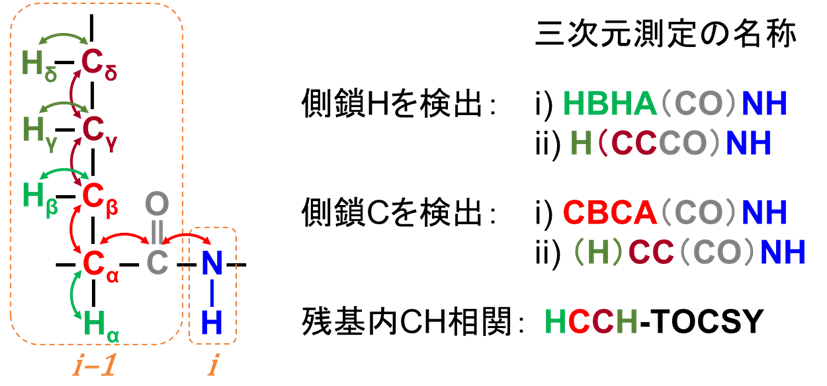
【図2】側鎖解析用三次元測定の磁化移動イメージおよび名称
図2のα位とβ位を帰属する手順の模式図を図3に示します。あるCH結合ピークに対して1H化学シフトと13C化学シフトの両方を知ることができれば1H-13C ctHSQCにおける位置を決定、すなわち帰属できます。1H-13C ctHSQC上に近接した複数の候補ピークがある場合は、残基内のCH相関を検出可能なHCCH-TOCSYを用いて、同一残基上のピークであることを確認した上で帰属します。
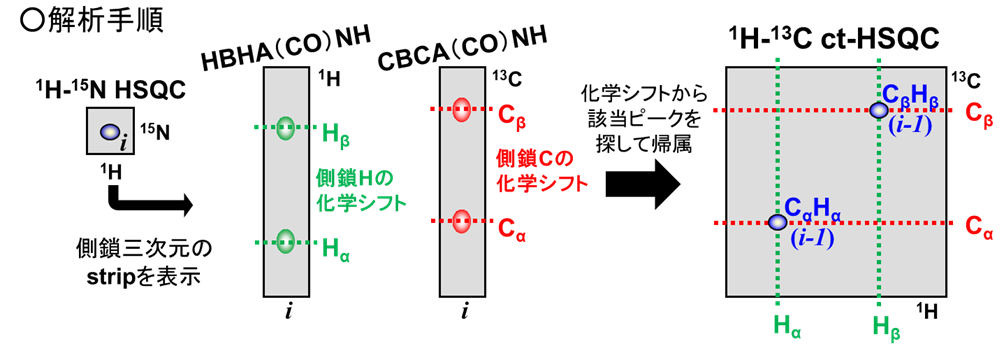
【図3】側鎖帰属の模式図
側鎖解析用三次元測定を用いて、アスパラギンやグルタミンの側鎖CH(α~γ位)の帰属から逆順でそれらの側鎖アミドNH2を帰属することも可能です。
③ 試料の側鎖解析結果
ここでは例として試料のHBHA(CO)NHおよびCBCA(CO)NHスペクトルを図4に示します。1.7mm Cryoプローブを用いると、GB1(6.3kDa)の場合約250μgの試料量で比較的短時間に解析可能なスペクトルが得られました。
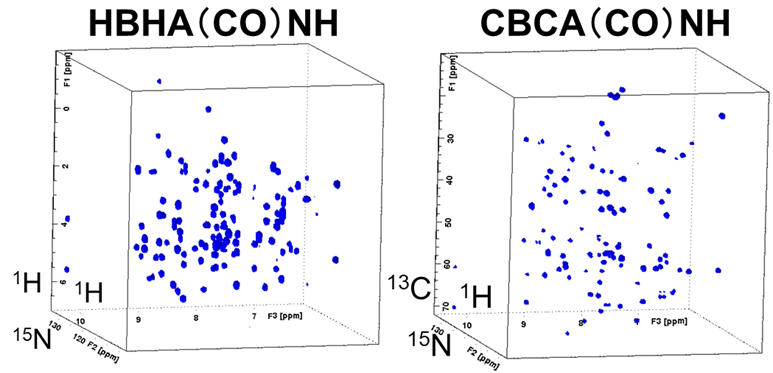
【図4】試料のHBHA(CO)NHおよびCBCA(CO)NHスペクトル
(測定時間:各3h、非線形サンプリング:12.5%)
最終的な側鎖解析結果の抜粋(1H-13C ctHSQCスペクトルより、α位およびメチル領域)を図5に示します。図5より、α位およびメチル基の完全な帰属が可能でした。
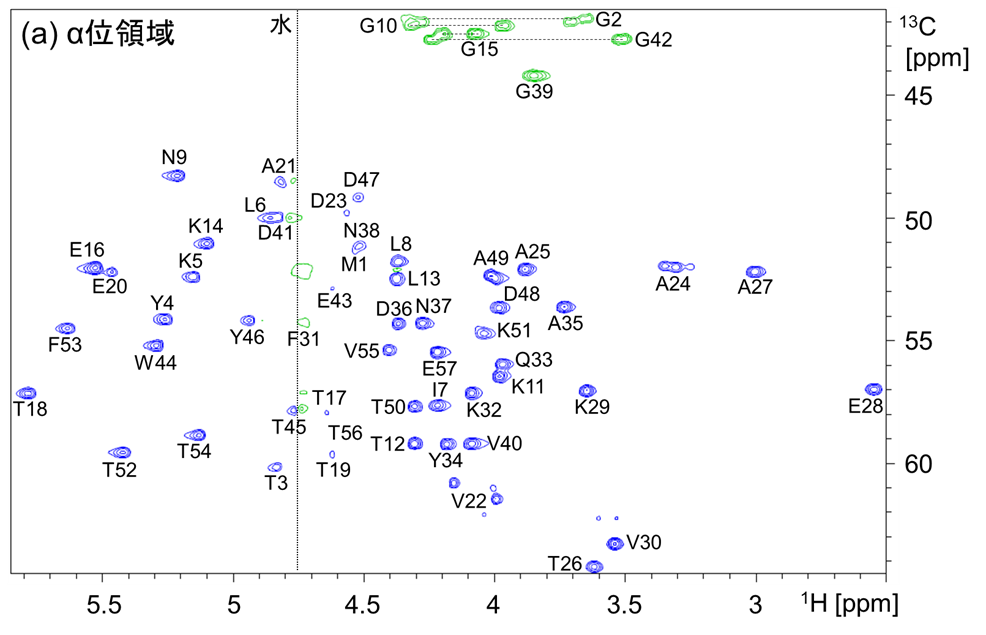
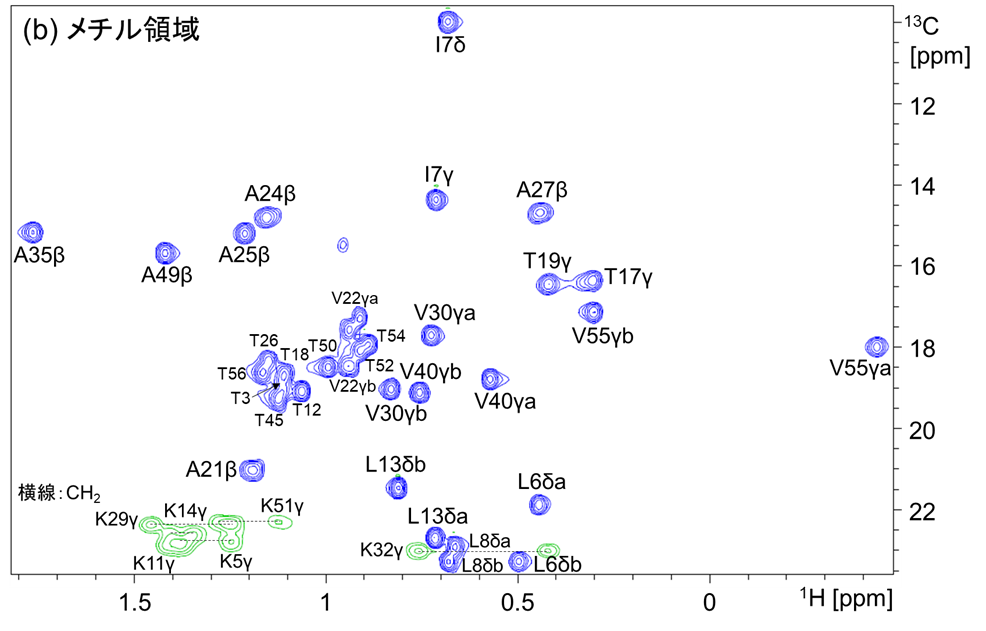
【図5】GB1の側鎖解析結果((a)α位領域、(b)メチル領域)
まとめ
溶液NMRによるタンパク質の側鎖解析では、1H-13C ctHSQCスペクトルの各ピークをタンパク質中の各CH結合に帰属します。本側鎖解析と主鎖解析の帰属情報がタンパク質の立体構造解析に必要となります。
